лЪЛђлЙл┤ЛЃл║ЛѓЛІ IVD Рђћ ЛЇЛѓлЙ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ лИ ЛЂлИЛЂЛѓлхл╝ЛІ, лИЛЂл┐лЙл╗ЛїлиЛЃлхл╝ЛІлх л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ, л╗лхЛЄлхлйлИЛЈ лИл╗лИ л┐ЛђлЙЛёлИл╗л░л║ЛѓлИл║лИ лил░л▒лЙл╗лхл▓л░лйлИл╣. лълйлИ л┐Лђлхл┤лйл░лилйл░ЛЄлхлйЛІ л┤л╗ЛЈ ЛЂл▒лЙЛђл░ лИ лИЛЂЛЂл╗лхл┤лЙл▓л░лйлИЛЈ л▒лИлЙл╗лЙл│лИЛЄлхЛЂл║лИЛЁ лЙл▒Лђл░лиЛєлЙл▓, Лѓл░л║лИЛЁ л║л░л║ л║ЛђлЙл▓Лї, ЛЂл╗Лјлйл░ лИл╗лИ Лѓл║л░лйлИ. лъл▒Лђл░лиЛєЛІ л╝лЙл│ЛЃЛѓ л▒ЛІЛѓЛї л▓лиЛЈЛѓЛІ лИли лйлЙЛЂл░ лИл╗лИ лил░л┤лйлхл╣ ЛЄл░ЛЂЛѓлИ л│лЙЛђл╗л░, л░ Лѓл░л║лХлх лИли л▓лхлйЛІ лИл╗лИ л┐л░л╗ЛїЛєл░.
лњл░лХлйлЙ лЙЛѓл╝лхЛѓлИЛѓЛї, ЛЄЛѓлЙ л┐ЛђлЙл┤ЛЃл║ЛѓЛІ IVD лйлхлИлйл▓л░лилИл▓лйЛІ. лЮл░л┐ЛђлИл╝лхЛђ,
Poclight HSCL-5000 Micro л│лЙл╝лЙл│лхлйлйЛІл╣ ЛЁлхл╝лИл╗Лјл╝лИлйлхЛЂЛєлхлйЛѓлйЛІл╣ лИл╝л╝ЛЃлйлЙЛёлхЛђл╝лхлйЛѓлйЛІл╣ л░лйл░л╗лИлил░ЛѓлЙЛђ
.
лъл┤лйл░л║лЙ лЙлйлИ л┐лЙ-л┐ЛђлхлХлйлхл╝ЛЃ ЛЂЛЄлИЛѓл░ЛјЛѓЛЂЛЈ л╝лхл┤лИЛєлИлйЛЂл║лИл╝лИ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░л╝лИ лИ л┐лЙЛЇЛѓлЙл╝ЛЃ л┐лЙл┤л╗лхлХл░Лѓ Лѓл░л║лЙл╝ЛЃ лХлх л║лЙлйЛѓЛђлЙл╗Лј. люлхл┤лИЛєлИлйЛЂл║лИлх ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ ЛЂлЙЛЂЛѓлЙЛЈЛѓ лИли л╗Лјл▒лЙл│лЙ лИлйЛЂЛѓЛђЛЃл╝лхлйЛѓл░, ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░, л┐ЛђлЙл│Лђл░л╝л╝лйлЙл│лЙ лЙл▒лхЛЂл┐лхЛЄлхлйлИЛЈ лИл╗лИ ЛЂл▓ЛЈлил░лйлйлЙл│лЙ ЛЂ лйлИл╝лИ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░, л┐Лђлхл┤лйл░лилйл░ЛЄлхлйлйлЙл│лЙ л┤л╗ЛЈ лИЛЂл┐лЙл╗ЛїлилЙл▓л░лйлИЛЈ л╗Лјл┤Лїл╝лИ ЛЂ Лєлхл╗ЛїЛј:
┬и
лћлИл░л│лйлЙЛЂЛѓлИл║л░, л┐ЛђлЙЛёлИл╗л░л║ЛѓлИл║л░, л╝лЙлйлИЛѓлЙЛђлИлйл│ лИл╗лИ л╗лхЛЄлхлйлИлх лил░л▒лЙл╗лхл▓л░лйлИл╣ лИл╗лИ ЛѓЛђл░л▓л╝.
┬и
лЪлЙл┤л┤лхЛђлХл║л░ лИл╗лИ ЛЂлЙЛЁЛђл░лйлхлйлИлх лХлИлилйлИ.
┬и
лалхл│ЛЃл╗лИЛђЛЃЛјЛЅл░ЛЈ л║лЙлйЛєлхл┐ЛєлИЛЈ.
┬и
лћлхлилИлйЛёлхл║ЛєлИЛЈ л╝лхл┤лИЛєлИлйЛЂл║лИЛЁ лИлил┤лхл╗лИл╣.
┬и
лЪЛђлхл┤лЙЛЂЛѓл░л▓л╗лхлйлИлх лИлйЛёлЙЛђл╝л░ЛєлИлИ л┤л╗ЛЈ л╝лхл┤лИЛєлИлйЛЂл║лИЛЁ Лєлхл╗лхл╣ л┐ЛЃЛѓлхл╝ ЛЂл▒лЙЛђл░ л▒лИлЙл╗лЙл│лИЛЄлхЛЂл║лИЛЁ лЙл▒Лђл░лиЛєлЙл▓ ЛЃ л╗Лјл┤лхл╣.
лЪЛђлЙлИлил▓лЙл┤лИЛѓлхл╗лИ ЛЂЛђлхл┤ЛЂЛѓл▓ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro л┤лЙл╗лХлйЛІ ЛЂлЙлЙЛѓл▓лхЛѓЛЂЛѓл▓лЙл▓л░ЛѓЛї лйлЙЛђл╝л░ЛѓлИл▓лйЛІл╝ ЛѓЛђлхл▒лЙл▓л░лйлИЛЈл╝ лЋл▓ЛђлЙл┐лхл╣ЛЂл║лЙл│лЙ ЛЂлЙЛјлил░, лњлхл╗лИл║лЙл▒ЛђлИЛѓл░лйлИлИ лИ лАлелљ л▓ лил░л▓лИЛЂлИл╝лЙЛЂЛѓлИ лЙЛѓ ЛђЛІлйл║л░, лйл░ л║лЙЛѓлЙЛђЛІл╣ лЙлйлИ ЛЁлЙЛѓЛЈЛѓ л▓ЛІл╣ЛѓлИ.
лГЛѓлИ ЛѓЛђлхл▒лЙл▓л░лйлИЛЈ л▓л║л╗ЛјЛЄл░ЛјЛѓ лЪлЙл╗лЙлХлхлйлИлх лЙ л┤лИл░л│лйлЙЛЂЛѓлИл║лх in vitro (IVDR) (лЋлА) 2017/746 л▓ лЋлА лИ лЪлЙл╗лЙлХлхлйлИлх лЙ л╝лхл┤лИЛєлИлйЛЂл║лИЛЁ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ЛЁ лњлхл╗лИл║лЙл▒ЛђлИЛѓл░лйлИлИ (UK MDR) 2002 л│лЙл┤л░ л▓ лњлхл╗лИл║лЙл▒ЛђлИЛѓл░лйлИлИ. лњ лАлЙлхл┤лИлйлхлйлйЛІЛЁ леЛѓл░Лѓл░ЛЁ лИлил┤лхл╗лИЛЈ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro лЙл┐Лђлхл┤лхл╗лхлйЛІ л▓ Лђл░лил┤лхл╗лх 201(h) лцлхл┤лхЛђл░л╗ЛїлйлЙл│лЙ лил░л║лЙлйл░ лЙ л┐лИЛЅлхл▓ЛІЛЁ л┐ЛђлЙл┤ЛЃл║Лѓл░ЛЁ, л╗лхл║л░ЛђЛЂЛѓл▓л░ЛЁ лИ л║лЙЛЂл╝лхЛѓлИЛЄлхЛЂл║лИЛЁ ЛЂЛђлхл┤ЛЂЛѓл▓л░ЛЁ (лЌл░л║лЙлй FD&C); ЛЇЛѓлИ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ Лѓл░л║лХлх л╝лЙл│ЛЃЛѓ л┐лЙл┤л┐л░л┤л░ЛѓЛї л┐лЙл┤ л┤лхл╣ЛЂЛѓл▓лИлх Лђл░лил┤лхл╗л░ 351 лЌл░л║лЙлйл░ лЙ ЛЂл╗ЛЃлХл▒лх лЙл▒ЛЅлхЛЂЛѓл▓лхлйлйлЙл│лЙ лил┤Лђл░л▓лЙлЙЛЁЛђл░лйлхлйлИЛЈ, л░ Лѓл░л║лХлх лЙЛѓлйлхЛЂлхлйлИЛЈ л║ л║л░Лѓлхл│лЙЛђлИЛЈл╝ л▓ ЛЂлЙлЙЛѓл▓лхЛѓЛЂЛѓл▓лИлИ ЛЂ лЪлЙл┐Лђл░л▓л║л░л╝лИ лЙл▒ ЛЃл╗ЛЃЛЄЛѕлхлйлИлИ л║л╗лИлйлИЛЄлхЛЂл║лИЛЁ л╗л░л▒лЙЛђл░ЛѓлЙЛђлИл╣ (CLIA) 1988 л│лЙл┤л░.
лњ ЛЂлЙлЙЛѓл▓лхЛѓЛЂЛѓл▓лИлИ ЛЂ IVDR лИлил┤лхл╗лИлх л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro лЙл┐Лђлхл┤лхл╗ЛЈлхЛѓЛЂЛЈ л║л░л║ ┬Фл╗Лјл▒лЙлх л╝лхл┤лИЛєлИлйЛЂл║лЙлх ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓лЙ, л║лЙЛѓлЙЛђлЙлх л┐Лђлхл┤ЛЂЛѓл░л▓л╗ЛЈлхЛѓ ЛЂлЙл▒лЙл╣ Лђлхл░л│лхлйЛѓ, л┐ЛђлЙл┤ЛЃл║Лѓ Лђлхл░л│лхлйЛѓл░, л║л░л╗лИл▒Лђл░ЛѓлЙЛђ, л║лЙлйЛѓЛђлЙл╗ЛїлйЛІл╣ л╝л░ЛѓлхЛђлИл░л╗, лйл░л▒лЙЛђ, лИлйЛЂЛѓЛђЛЃл╝лхлйЛѓ, л░л┐л┐л░Лђл░Лѓ, ЛЄл░ЛЂЛѓЛї лЙл▒лЙЛђЛЃл┤лЙл▓л░лйлИЛЈ, л┐ЛђлЙл│Лђл░л╝л╝лйлЙлх лЙл▒лхЛЂл┐лхЛЄлхлйлИлх лИл╗лИ ЛЂлИЛЂЛѓлхл╝ЛЃ, лйлхлил░л▓лИЛЂлИл╝лЙ лЙЛѓ ЛѓлЙл│лЙ, лИЛЂл┐лЙл╗ЛїлиЛЃЛјЛѓЛЂЛЈ л╗лИ лЙлйлИ лЙЛѓл┤лхл╗ЛїлйлЙ лИл╗лИ л▓ л║лЙл╝л▒лИлйл░ЛєлИлИ, л┐Лђлхл┤лйл░лилйл░ЛЄлхлйлйЛІлх л┤л╗ЛЈ л┐ЛђлЙлИлил▓лЙл┤лИЛѓлхл╗лхл╝ л┤л╗ЛЈ лИЛЂл┐лЙл╗ЛїлилЙл▓л░лйлИЛЈ in vitro л┤л╗ЛЈ лИЛЂЛЂл╗лхл┤лЙл▓л░лйлИЛЈ лЙл▒Лђл░лиЛєлЙл▓, л▓л║л╗ЛјЛЄл░ЛЈ л┤лЙлйлЙЛђЛЂл║ЛЃЛј л║ЛђлЙл▓Лї лИ Лѓл║л░лйлИ, л┐лЙл╗ЛЃЛЄлхлйлйЛІлх лИли ЛЄлхл╗лЙл▓лхЛЄлхЛЂл║лЙл│лЙ Лѓлхл╗л░Рђд┬╗
лЪлЙ лЙЛєлхлйл║л░л╝ ЛЇл║ЛЂл┐лхЛђЛѓлЙл▓, л┐ЛђлИл╝лхЛђлйлЙ 70% л▓ЛЂлхЛЁ л║л╗лИлйлИЛЄлхЛЂл║лИЛЁ ЛђлхЛѕлхлйлИл╣ л┐ЛђлИлйлИл╝л░ЛјЛѓЛЂЛЈ ЛЂ лИЛЂл┐лЙл╗ЛїлилЙл▓л░лйлИлхл╝ лИлил┤лхл╗лИл╣ IVD.
лЪЛђлИл╝лхЛђЛІ лИлил┤лхл╗лИл╣ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro
лблхЛЂЛѓЛІ лйл░ л▒лхЛђлхл╝лхлйлйлЙЛЂЛѓЛї, ЛѓлхЛЂЛѓЛІ лйл░ COVID-19 лИ ЛѓлхЛЂЛѓЛІ лйл░ лњлўлД ЛЈл▓л╗ЛЈЛјЛѓЛЂЛЈ л┐ЛђлИл╝лхЛђл░л╝лИ л┐ЛђлЙл┤ЛЃл║ЛѓлЙл▓ IVD. лћЛђЛЃл│лИлх л┐ЛђлИл╝лхЛђЛІ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓ Poclight HSCL-5000 Micro CLIA Analyzer IVD л▓л║л╗ЛјЛЄл░ЛјЛѓ:
┬и
лћлИл░л│лйлЙЛЂЛѓлИл║л░ Лђл░л║л░
┬и лћлИл░л│лйлЙЛЂЛѓлИл║л░ ЛЅлИЛѓлЙл▓лИл┤лйлЙл╣ лХлхл╗лхлиЛІ
┬и лћлИл░л│лйлЙЛЂЛѓлИл║л░ л▓лЙЛЂл┐л░л╗лхлйлИЛЈ
┬и
лўл╝л╝ЛЃлйлЙл░лйл░л╗лИлиЛІ
┬и ...
лАлЙЛЂЛЃл┤ЛІ, лИлил│лЙЛѓлЙл▓л╗лхлйлйЛІлх л┤л╗ЛЈ л╝лхл┤лИЛєлИлйЛЂл║лИЛЁ лЙл▒Лђл░лиЛєлЙл▓, Лѓл░л║лХлх ЛЈл▓л╗ЛЈЛјЛѓЛЂЛЈ лИлил┤лхл╗лИЛЈл╝лИ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro. лЪлЙ л┤л░лйлйЛІл╝ лњЛЂлхл╝лИЛђлйлЙл╣ лЙЛђл│л░лйлИлил░ЛєлИлИ лил┤Лђл░л▓лЙлЙЛЁЛђл░лйлхлйлИЛЈ, ЛЂлхл│лЙл┤лйЛЈ л┤л╗ЛЈ ЛѓлхЛЂЛѓлИЛђлЙл▓л░лйлИЛЈ IVD л┤лЙЛЂЛѓЛЃл┐лйлЙ л▒лЙл╗лхлх 40 000 л┐ЛђлЙл┤ЛЃл║ЛѓлЙл▓. лълйлИ л╝лЙл│ЛЃЛѓ л▓л░ЛђЛїлИЛђлЙл▓л░ЛѓЛїЛЂЛЈ лЙЛѓ ЛѓЛђл░л┤лИЛєлИлЙлйлйЛІЛЁ л╗л░л▒лЙЛђл░ЛѓлЙЛђлйЛІЛЁ ЛѓлхЛЂЛѓлЙл▓ л┤лЙ ЛѓлхЛЂЛѓлЙл▓ л┐лЙ л╝лхЛЂЛѓЛЃ лЙл║л░лил░лйлИЛЈ л╝лхл┤лИЛєлИлйЛЂл║лЙл╣ л┐лЙл╝лЙЛЅлИ.
лџл╗л░ЛЂЛЂлИЛёлИл║л░ЛєлИЛЈ IVD
лњ лАлЙлхл┤лИлйлхлйлйЛІЛЁ леЛѓл░Лѓл░ЛЁ лБл┐Лђл░л▓л╗лхлйлИлх л┐лЙ ЛЂл░лйлИЛѓл░ЛђлйлЙл╝ЛЃ лйл░л┤лилЙЛђЛЃ лил░ л║л░ЛЄлхЛЂЛѓл▓лЙл╝ л┐лИЛЅлхл▓ЛІЛЁ л┐ЛђлЙл┤ЛЃл║ЛѓлЙл▓ лИ л╝лхл┤лИл║л░л╝лхлйЛѓлЙл▓ (FDA) лЙЛѓлйлЙЛЂлИЛѓ л▓ЛЂлх л╝лхл┤лИЛєлИлйЛЂл║лИлх ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░, л▓л║л╗ЛјЛЄл░ЛЈ лИлил┤лхл╗лИЛЈ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro, л║ л║л╗л░ЛЂЛЂЛЃ I, л║л╗л░ЛЂЛЂЛЃ II лИл╗лИ л║л╗л░ЛЂЛЂЛЃ III. лџл╗л░ЛЂЛЂлИЛёлИл║л░ЛєлИЛЈ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ л▒ЛЃл┤лхЛѓ л▓л░ЛђЛїлИЛђлЙл▓л░ЛѓЛїЛЂЛЈ л▓ лил░л▓лИЛЂлИл╝лЙЛЂЛѓлИ лЙЛѓ ЛЂл▓ЛЈлил░лйлйлЙл│лЙ ЛЂ лйлИл╝ ЛђлИЛЂл║л░ лИ ЛЃЛђлЙл▓лйЛЈ лйлЙЛђл╝л░ЛѓлИл▓лйлЙл│лЙ л║лЙлйЛѓЛђлЙл╗ЛЈ, лйлхлЙл▒ЛЁлЙл┤лИл╝лЙл│лЙ л┤л╗ЛЈ лЙл▒лхЛЂл┐лхЛЄлхлйлИЛЈ л▒лхлилЙл┐л░ЛЂлйлЙЛЂЛѓлИ л┐ЛђлЙл┤ЛЃл║Лѓл░. лАлЙлЙЛѓл▓лхЛѓЛЂЛѓл▓лхлйлйлЙ, л║л╗л░ЛЂЛЂлИЛёлИл║л░ЛєлИЛЈ IVD л▒ЛЃл┤лхЛѓ лЙл┐Лђлхл┤лхл╗ЛЈЛѓЛї л┐Лђлхл┤ЛђЛІлйлЙЛЄлйЛІл╣ л┐ЛђлЙЛєлхЛЂЛЂ, л║лЙЛѓлЙЛђлЙл╝ЛЃ л┤лЙл╗лХлхлй ЛЂл╗лхл┤лЙл▓л░ЛѓЛї л┐ЛђлЙлИлил▓лЙл┤лИЛѓлхл╗Лї, ЛЄЛѓлЙл▒ЛІ л▓ЛІл▓лхЛЂЛѓлИ ЛЂл▓лЙл╣ л┐ЛђлЙл┤ЛЃл║Лѓ лйл░ ЛђЛІлйлЙл║.
┬и
лЪЛђлЙл┤ЛЃл║ЛѓЛІ л║л╗л░ЛЂЛЂл░ I лЙЛѓлйлЙЛЂЛЈЛѓЛЂЛЈ л║ л║л░Лѓлхл│лЙЛђлИлИ ЛђлИЛЂл║л░ лЙЛѓ лйлИлил║лЙл│лЙ л┤лЙ ЛЃл╝лхЛђлхлйлйлЙл│лЙ лИ ЛѓЛђлхл▒ЛЃЛјЛѓ лЙл▒ЛЅлхл│лЙ л║лЙлйЛѓЛђлЙл╗ЛЈ.
┬и
лЪЛђлЙл┤ЛЃл║ЛѓЛІ л║л╗л░ЛЂЛЂл░ II ЛЂЛЄлИЛѓл░ЛјЛѓЛЂЛЈ ЛђлИЛЂл║лЙл╝ лЙЛѓ ЛЃл╝лхЛђлхлйлйлЙл│лЙ л┤лЙ л▓ЛІЛЂлЙл║лЙл│лЙ лИ ЛѓЛђлхл▒ЛЃЛјЛѓ лЙл▒ЛЅлхл│лЙ л║лЙлйЛѓЛђлЙл╗ЛЈ лИ ЛЂл┐лхЛєлИл░л╗ЛїлйлЙл│лЙ л║лЙлйЛѓЛђлЙл╗ЛЈ.
┬и
лЪЛђлЙл┤ЛЃл║ЛѓЛІ л║л╗л░ЛЂЛЂл░ III ЛЂЛЄлИЛѓл░ЛјЛѓЛЂЛЈ л┐ЛђлЙл┤ЛЃл║Лѓл░л╝лИ ЛЂ л▓ЛІЛЂлЙл║лИл╝ ЛђлИЛЂл║лЙл╝ лИ ЛѓЛђлхл▒ЛЃЛјЛѓ лЙл▒ЛЅлхл│лЙ л║лЙлйЛѓЛђлЙл╗ЛЈ лИ л┐Лђлхл┤л┐ЛђлЙл┤л░лХлйлЙл│лЙ лЙл┤лЙл▒ЛђлхлйлИЛЈ (PMA).
лњл░лХлйлЙ лЙЛѓл╝лхЛѓлИЛѓЛї, ЛЄЛѓлЙ л┐лЙ л╝лхЛђлх ЛЃл▓лхл╗лИЛЄлхлйлИЛЈ л║л╗л░ЛЂЛЂл░ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ ЛЃл▓лхл╗лИЛЄлИл▓л░лхЛѓЛЂЛЈ лИ лйлЙЛђл╝л░ЛѓлИл▓лйЛІл╣ л║лЙлйЛѓЛђлЙл╗Лї. лБЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ IVR л║л╗л░ЛЂЛЂл░ I л┐лЙл┤л╗лхлХл░Лѓ лйл░лИл╝лхлйЛїЛѕлхл╝ЛЃ лйлЙЛђл╝л░ЛѓлИл▓лйлЙл╝ЛЃ л║лЙлйЛѓЛђлЙл╗Лј, л▓ ЛѓлЙ л▓Лђлхл╝ЛЈ л║л░л║ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ IVR л║л╗л░ЛЂЛЂл░ III л┐Лђлхл┤ЛіЛЈл▓л╗ЛЈЛјЛѓ ЛЂл░л╝ЛІлх ЛЂЛѓЛђлЙл│лИлх ЛѓЛђлхл▒лЙл▓л░лйлИЛЈ. люлхл┤лИл║лЙ-л▒лИлЙл╗лЙл│лИЛЄлхЛЂл║лИлх л║лЙл╝л┐л░лйлИлИ, лХлхл╗л░ЛјЛЅлИлх л▓ЛІл▓лхЛЂЛѓлИ ЛЂл▓лЙлИ л┐ЛђлЙл┤ЛЃл║ЛѓЛІ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro лйл░ ЛђЛІлйлЙл║ лАлелљ, л╝лЙл│ЛЃЛѓ лЙл▒Лђл░ЛѓлИЛѓЛїЛЂЛЈ л║ ЛђлхЛЂЛЃЛђЛЂЛЃ FDA ┬Флџл╗л░ЛЂЛЂлИЛёлИЛєлИЛђЛЃл╣Лѓлх л▓л░Лѕлх л╝лхл┤лИЛєлИлйЛЂл║лЙлх ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓лЙ┬╗.
лЦлЙЛѓлИЛѓлх лЙл▒лхЛЂл┐лхЛЄлИЛѓЛї ЛЂлЙл▒л╗Лјл┤лхлйлИлх лйлЙЛђл╝л░ЛѓлИл▓лйЛІЛЁ ЛѓЛђлхл▒лЙл▓л░лйлИл╣ л▓ лЋл▓ЛђлЙл┐лхл╣ЛЂл║лЙл╝ лАлЙЛјлилх? лњ 2021 л│лЙл┤ЛЃ IVDR л▒ЛІл╗ лЙл▒лйлЙл▓л╗лхлй лИ л▓л║л╗ЛјЛЄл░лхЛѓ Лѓл░л║лИлх ЛЃл╗ЛЃЛЄЛѕлхлйлИЛЈ, л║л░л║:
┬и
лДлхЛѓл║лИлх лЙл▒ЛЈлил░Лѓлхл╗ЛїЛЂЛѓл▓л░ л┤л╗ЛЈ л┐ЛђлЙлИлил▓лЙл┤лИЛѓлхл╗лхл╣, лИл╝л┐лЙЛђЛѓлхЛђлЙл▓ лИ л┤лИЛЂЛѓЛђлИл▒ЛїЛјЛѓлЙЛђлЙл▓, л║л░ЛЂл░ЛјЛЅлИлхЛЂЛЈ лЙЛѓЛЂл╗лхлХлИл▓л░лйлИЛЈ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓, Лђлхл│лИЛЂЛѓЛђл░ЛєлИлИ лИ л┐ЛђлЙл▓лхЛђл║лИ лйл░л┤л╗лхлХл░ЛЅлхл╣ л╝л░Лђл║лИЛђлЙл▓л║лИ. лГЛѓлЙ л▓л║л╗ЛјЛЄл░лхЛѓ л▓ ЛЂлхл▒ЛЈ ЛЂлИЛЂЛѓлхл╝ЛЃ лЙЛѓЛЂл╗лхлХлИл▓л░лйлИЛЈ, лЙЛЂлйлЙл▓л░лйлйЛЃЛј лйл░ ЛЃлйлИл║л░л╗ЛїлйлЙл╝ лИл┤лхлйЛѓлИЛёлИл║л░ЛѓлЙЛђлх ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ (UDI).
┬и
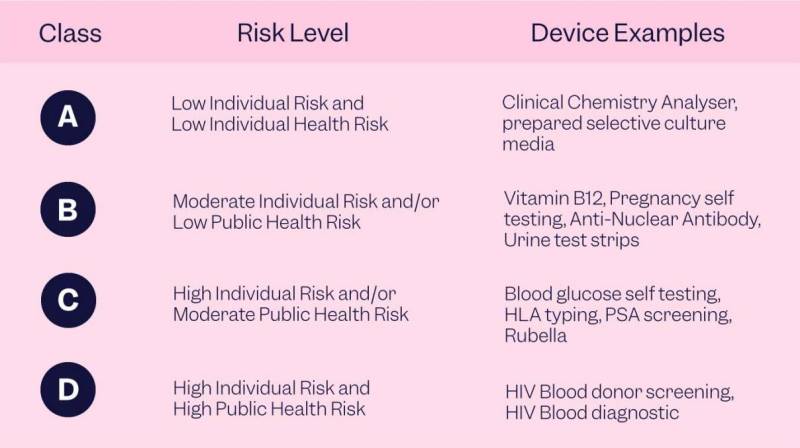
лњл▓лхл┤лхлйлИлх л║л╗л░ЛЂЛЂлИЛёлИл║л░ЛєлИлИ, ЛЂлЙЛЂЛѓлЙЛЈЛЅлхл╣ лИли ЛЄлхЛѓЛІЛђлхЛЁ л║л╗л░ЛЂЛЂлЙл▓ ЛђлИЛЂл║л░. лБЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ л║л╗л░ЛЂЛЂл░ A ЛЁл░Лђл░л║ЛѓлхЛђлИлиЛЃЛјЛѓЛЂЛЈ лйлИлил║лИл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лил┤лЙЛђлЙл▓ЛїЛЈ ЛЄлхл╗лЙл▓лхл║л░ лИ лйл░ЛЂлхл╗лхлйлИЛЈ, ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ л║л╗л░ЛЂЛЂл░ B ЛЁл░Лђл░л║ЛѓлхЛђлИлиЛЃЛјЛѓЛЂЛЈ ЛЃл╝лхЛђлхлйлйЛІл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лил┤лЙЛђлЙл▓ЛїЛЈ ЛЄлхл╗лЙл▓лхл║л░ лИ/лИл╗лИ лйлИлил║лИл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лил┤лЙЛђлЙл▓ЛїЛЈ лйл░ЛЂлхл╗лхлйлИЛЈ, ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ л║л╗л░ЛЂЛЂл░ C ЛЁл░Лђл░л║ЛѓлхЛђлИлиЛЃЛјЛѓЛЂЛЈ л▓ЛІЛЂлЙл║лИл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лЙЛѓл┤лхл╗ЛїлйлЙл│лЙ ЛЄлхл╗лЙл▓лхл║л░ лИ/лИл╗лИ ЛЃл╝лхЛђлхлйлйЛІл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лил┤лЙЛђлЙл▓ЛїЛЈ лйл░ЛЂлхл╗лхлйлИЛЈ, л░ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░ л║л╗л░ЛЂЛЂл░ D ЛЁл░Лђл░л║ЛѓлхЛђлИлиЛЃЛјЛѓЛЂЛЈ л▓ЛІЛЂлЙл║лИл╝ ЛђлИЛЂл║лЙл╝ л┤л╗ЛЈ лЙЛѓл┤лхл╗ЛїлйлЙл│лЙ ЛЄлхл╗лЙл▓лхл║л░ лИ л▓ЛІЛЂлЙл║лИл╝ ЛЃЛђлЙл▓лйлхл╝ ЛђлИЛЂл║л░. ЛђлИЛЂл║ л┤л╗ЛЈ лил┤лЙЛђлЙл▓ЛїЛЈ лйл░ЛЂлхл╗лхлйлИЛЈ.
┬и
лЉлЙл╗лхлх ЛЂЛѓЛђлЙл│лИл╣ л║лЙлйЛѓЛђлЙл╗Лї лил░ IVD-ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░л╝лИ л▓ЛІЛЂлЙл║лЙл│лЙ ЛђлИЛЂл║л░.
┬и
лЊл░Лђл░лйЛѓлИЛђлЙл▓л░лйлйЛІл╣ лйл░л┤лилЙЛђ лйлЙЛѓлИЛёлИЛєлИЛђлЙл▓л░лйлйЛІЛЁ лЙЛђл│л░лйлЙл▓ (лИл╗лИ лйлхлил░л▓лИЛЂлИл╝ЛІЛЁ ЛЂЛѓлЙЛђлЙлйлйлИЛЁ лЙЛђл│л░лйлЙл▓ л┐лЙ лЙЛєлхлйл║лх ЛЂлЙлЙЛѓл▓лхЛѓЛЂЛѓл▓лИЛЈ) лил░ ЛЂЛЄлхЛѓ ЛЃЛЂлИл╗лхлйлИЛЈ лЙл┐Лђлхл┤лхл╗лхлйлйлЙл│лЙ лйл░л▒лЙЛђл░ л║ЛђлИЛѓлхЛђлИлхл▓.
┬и
лЉлЙл╗ЛїЛѕл░ЛЈ л┐ЛђлЙлиЛђл░ЛЄлйлЙЛЂЛѓЛї ЛЂ лЙл▒ЛѕлИЛђлйлЙл╣ л▒л░лилЙл╣ л┤л░лйлйЛІЛЁ л┐лЙ л╝лхл┤лИЛєлИлйЛЂл║лИл╝ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░л╝ л▓ лЋлА (л┐лЙл┤ лйл░лил▓л░лйлИлхл╝ EUDAMED).
┬и
лБЛЂлИл╗лхлйлйЛІлх л║л╗лИлйлИЛЄлхЛЂл║лИлх л┤лЙл║л░лил░Лѓлхл╗ЛїЛЂЛѓл▓л░ лИ л┐Лђл░л▓лИл╗л░ лЙЛєлхлйл║лИ ЛЇЛёЛёлхл║ЛѓлИл▓лйлЙЛЂЛѓлИ ЛЂ л▒лЙл╗ЛїЛѕлхл╣ л║лЙлЙЛђл┤лИлйл░ЛєлИлхл╣ л╝лхлХл┤ЛЃ ЛЂЛѓЛђл░лйл░л╝лИ лЋлА, лЙЛЂлЙл▒лхлйлйлЙ л▓ ЛѓлЙл╝, ЛЄЛѓлЙ л║л░ЛЂл░лхЛѓЛЂЛЈ лйл░л┤лилЙЛђл░ лил░ ЛђЛІлйл║лЙл╝.
┬и
лЉлЙл╗лхлх ЛЂЛѓЛђлЙл│лИлх ЛѓЛђлхл▒лЙл▓л░лйлИЛЈ л┐ЛђлЙлИлил▓лЙл┤лИЛѓлхл╗ЛЈ л║ л┐лЙЛЂл╗лхл┐ЛђлЙл┤л░лХлйлЙл╝ЛЃ лйл░л┤лилЙЛђЛЃ.
┬и
лъЛЂлЙл▒ЛІлх ЛѓЛђлхл▒лЙл▓л░лйлИЛЈ л║ ┬Фл▓лйЛЃЛѓЛђлхлйлйлИл╝ ЛЃЛЂЛѓЛђлЙл╣ЛЂЛѓл▓л░л╝┬╗ лИл╗лИ лИлил┤лхл╗лИЛЈл╝ л┤л╗ЛЈ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ in vitro, л┐ЛђлЙлИлил▓лЙл┤лИл╝ЛІл╝ лИ лИЛЂл┐лЙл╗ЛїлиЛЃлхл╝ЛІл╝ л▓ лЙл┤лйлЙл╝ лИ ЛѓлЙл╝ лХлх ЛЃЛЄЛђлхлХл┤лхлйлИлИ.
лџл╗ЛјЛЄлхл▓ЛІл╝ л╝лЙл╝лхлйЛѓлЙл╝ ЛЈл▓л╗ЛЈлхЛѓЛЂЛЈ л▒лхлилЙл┐л░ЛЂлйЛІл╣ лИ ЛЇЛёЛёлхл║ЛѓлИл▓лйЛІл╣ л▓ЛІл▓лЙл┤ IVD-л┐ЛђлЙл┤ЛЃл║Лѓл░ лйл░ ЛђЛІлйлЙл║, л░ л┐лЙлйлИл╝л░лйлИлх л┤лхл╣ЛЂЛѓл▓ЛЃЛјЛЅлИЛЁ л┐Лђл░л▓лИл╗ Рђћ лИл┤лхл░л╗ЛїлйЛІл╣ л┐лхЛђл▓ЛІл╣ Лѕл░л│.
лњЛІл▓лЙл┤
лЪЛђлЙл┤ЛЃл║ЛѓЛІ IVD ЛЈл▓л╗ЛЈЛјЛѓЛЂЛЈ л▓л░лХлйлЙл╣ л╗лИлйлИлхл╣ лил░ЛЅлИЛѓЛІ лЙЛѓ Лђл░лил╗лИЛЄлйЛІЛЁ лил░л▒лЙл╗лхл▓л░лйлИл╣. лЉлхлилЙл┐л░ЛЂлйлЙЛЂЛѓЛї лИ л║л░ЛЄлхЛЂЛѓл▓лЙ л┤лИл░л│лйлЙЛЂЛѓлИл║лИ In Vitro л║Лђл░л╣лйлх л▓л░лХлйЛІ, лИ лИл╝лхлйлйлЙ л┐лЙЛЇЛѓлЙл╝ЛЃ ЛЂлЙл▒л╗Лјл┤лхлйлИлх лйлЙЛђл╝л░ЛѓлИл▓лйЛІЛЁ ЛѓЛђлхл▒лЙл▓л░лйлИл╣ л┐ЛђлЙлИлил▓лЙл┤лИЛѓлхл╗ЛЈ Лѓл░л║ л▓л░лХлйлЙ. Poclight лИл╝лхлхЛѓ ЛЂлхЛђЛѓлИЛёлИл║л░ЛѓЛІ CE лИ ISO лИ лИл╝лхлхЛѓ л┐лЙл╗лйЛІл╣ лйл░л▒лЙЛђ Лђлхл░л│лхлйЛѓлЙл▓, ЛЄЛѓлЙл▒ЛІ ЛЂл┤лхл╗л░ЛѓЛї ЛѓлхЛЂЛѓлИЛђлЙл▓л░лйлИлх л▒лхлилил░л▒лЙЛѓлйЛІл╝.

 English
English fran├Дais
fran├Дais ЛђЛЃЛЂЛЂл║лИл╣
ЛђЛЃЛЂЛЂл║лИл╣ espa├▒ol
espa├▒ol portugu├фs
portugu├фs пД┘ёп╣п▒пе┘іпЕ
пД┘ёп╣п▒пе┘іпЕ ТЌЦТюгУфъ
ТЌЦТюгУфъ T├╝rk├Дe
T├╝rk├Дe Яц╣Яц┐ЯцѓЯцдЯЦђ
Яц╣Яц┐ЯцѓЯцдЯЦђ Indonesia
Indonesia 







 Specated Ipv6 Network |
Specated Ipv6 Network | 